Exercício Resolvido de Calorimetria
publicidade
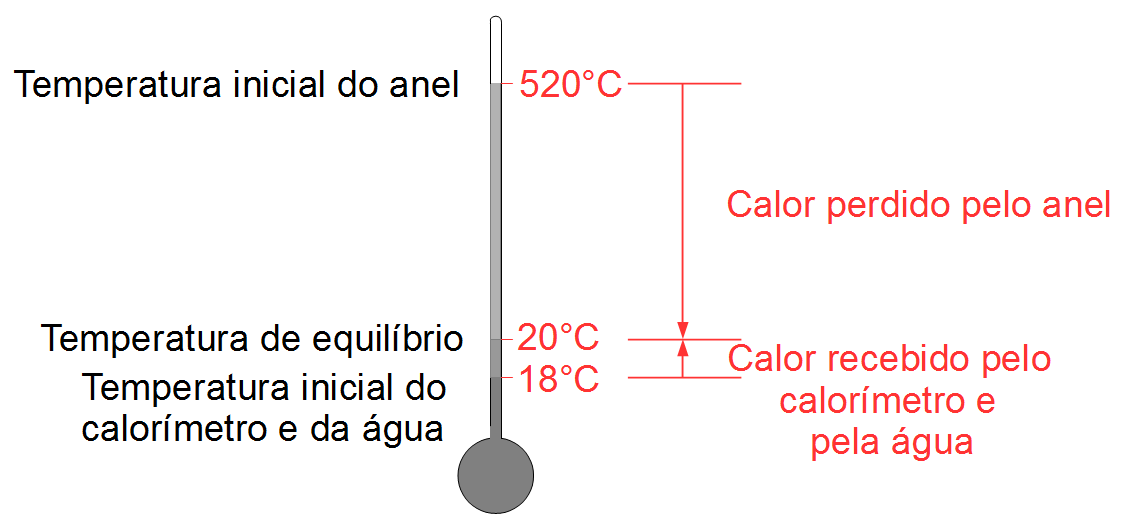
Um rapaz comprou um anel onde dizia ter 9 gramas de ouro e 1 grama de cobre. Para comprovar a informação, o rapaz, um estudante de física, aqueceu o anel (que realmente tinha 10 gramas de massa) até 520 °C, que sabia ser inferior ao ponto de fusão dos dois metais. Colocou o anel em um calorímetro de capacidade térmica 20 cal/°C e que continha 80 gramas de água a 18 °C. O equilíbrio térmico se verificou a 20 °C. Supondo que na ligas os calores específicos sejam 0,09 cal/g°C para o cobre e 0,03 cal/g°C para o ouro, determine as massa de cobre e ouro existentes no anel.
Dados do problema:
- Massa do anel: M = 10 g;
- Temperatura inicial do anel: ta = 520 °C;
- Calor específico do cobre: cCu = 0,09 cal/g°C;
- Calor específico do ouro: cAu = 0,03 cal/g°C;
- Capacidade térmica do calorímetro: C = 20 cal/°C;
- Temperatura inicial di calorímetro: tc = 18 °C;
- Massa de água: ma = 80 g;
- Temperatura inicial da água: ta = 18 °C;
- Temperatura de equilíbrio: teq = 20 °C;
- Adotando o calor específico da água: ca = 1 cal/g°C.
| m(g) | c(cal/g°C) | ti(°C) | teq(°C) | |
|---|---|---|---|---|
| Calorímetro | 20 cal/°C | 18 | 20 | |
| Água | 80 | 1 | 18 | 20 |
| Anel | 10 | c | 520 | 20 |
Tabela 1
onde c é o calor específico do anel.
Observação: Não conhecemos a massa e o calor específico do calorímetro, mas conhecemos sua
capacidade térmica C, que é dada pelo produto da massa multiplicada pelo calor específico
\( C=mc=20\;\text{cal/g°C} \).
Solução
Calores trocados em cada elemento:
- Calorímetro
\[
\begin{gather}
\bbox[#99CCFF,10px]
{Q=mc\left(t_{eq}-t_{0}\right)} \tag{I}
\end{gather}
\]
A capacidade térmica é dada por
\[
\begin{gather}
\bbox[#99CCFF,10px]
{C=mc} \tag{II}
\end{gather}
\]
substituindo a expressão (II) na expressão (I)
\[
\begin{gather}
Q_{C}=C\left(t_{eq}-t_{0}\right)\\
Q_{C}=20.(20-18)\\
Q_{C}=20.2\\
Q_{C}=40\;\text{cal}
\end{gather}
\]
- Água
\[
\begin{gather}
Q_{a}=80.1.\left(20-18\right)\\
Q_{a}=80.2\\
Q_{a}=160\;\text{cal/g°C}
\end{gather}
\]
- Anel
\[
\begin{gather}
Q_{n}=10c\left(20-520\right)\\
Q_{n}=-500.10c\\
Q_{n}=-5000c
\end{gather}
\]
A somatória dos calores trocados é igual a zero
\[
\begin{gather}
\sum Q=0\\
Q_{C}+Q_{a}+Q_{n}=0\\
40+160-5000c=0\\
5000c=200\\
c-\frac{200}{5000}\\
c=0,04\;\text{cal/g°C}
\end{gather} \tag{III}
\]
Este é o calor específico da liga metálica de ouro e cobre. O calor específico da liga, em função dos
calores específicos e das frações de massa de cada um dos metais que constituem a liga, é dado por
\[
\begin{gather}
c=c_{Au}\frac{m_{Au}}{M}+c_{Cu}\frac{m_{Cu}}{M} \tag{IV}
\end{gather}
\]
onde M é a massa total da liga metálica
\[
M=m_{Au}+m_{Cu}
\]
substituindo a massa total dada no problema e escrendo a massa de ouro em função da massa de cobre
\[
\begin{gather}
10=m_{Au}+m_{Cu}\\
m_{Au}=10-m_{Cu} \tag{V}
\end{gather}
\]
substituindo o valor encontrado em (III), os dados do problema e a expressão (V) na expressão (IV)
\[
0,04=0,03.\frac{(10-m_{Cu})}{10}+0,09.\frac{m_{Cu}}{10}
\]
multiplicando toda a equação por 10
\[
\begin{gather}
\qquad\qquad 0,04=0,03.\frac{(10-m_{Cu})}{10}+0,09.\frac{m_{Cu}}{10}\qquad (\times10)\\
0,04.10=0,03.\frac{(10-m_{Cu})}{10}.10+0,09.\frac{m_{Cu}}{10}.10\\
0,4=0,03.(10-m_{Cu})+0,09m_{Cu}\\
0,4=0,3-0,03m_{Cu}+0,09m_{Cu}\\
0,06m_{Cu}=0,4-0,3\\
0,06m_{Cu}=0,1\\
m_{Cu}=\frac{0,1}{0,06}
\end{gather}
\]
\[ \bbox[#FFCCCC,10px]
{m_{Cu}\approx 1,7\;\text{g}}
\]
substituindo este resultado na expressão (V)
\[
m_{Au}=10-1,7
\]
\[ \bbox[#FFCCCC,10px]
{m_{Au}\approx 8,3\;\text{g}}
\]
Observação: A expressão (IV) é a Lei de Kopp ou regra de Neumann-Kopp para o
cálculo do calor específico de uma liga metálica formada por dois elementos. Genericamente para n
elementos em uma liga
\[ \bbox[#99CCFF,10px]
{c=\sum _{i=1}^{n}c_{i}f_{i}\ \ \ ,\ \ \ f_{i}=\frac{m_{i}}{m}}
\]
onde c é o calor específico da liga metálica, ci é o calor específico do
i-ésimo elemento e fi é a fração de massa do i-ésimo elemento (massa
do elemento na liga dividido pela massa total da amostra).
publicidade

Fisicaexe - Exercícios Resolvidos de Física de Elcio Brandani Mondadori está licenciado com uma Licença Creative Commons - Atribuição-NãoComercial-Compartilha Igual 4.0 Internacional .