Exercício Resolvido de Calorimetria
publicidade
De que altura deveria cair uma determinada massa de água para que a sua energia final, convertida em calor, aumentasse a temperatura dessa massa de 1 °C? Admita não haver perdas.
Dados: 1 cal = 4,18 J, g = 9,8 m/s2, c = 1 cal/g°C.
Dados do problema:
- Variação da temperatura da água: Δ t = 1 °C;
- Calor específico da água: c = 1 cal/g°C;
- Equivalente mecânico do calor: 1 cal = 4,18 J;
- Aceleração da gravidade: g = 9,8 m/s2.
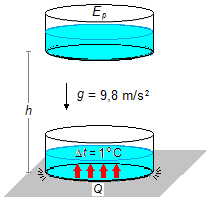
Na posição inicial, a uma altura h, toda a energia mecânica da massa de água está na forma de
energia potencial EP. Quando a massa atinge o solo, admitindo que não haja perda de
energia, toda a energia potencial se converte em calor Q que aquece a água (Figura 1).
Em primeiro lugar devemos converter o calor específico da água dado em calorias por grama-grau Celsius (cal/g°C) para joules por quilograma-grau Celsius (J/kg°C) usado no Sistema Internacional de Unidades (S.I.)
\[
\begin{gather}
c=1\;\mathrm{\frac{\cancel{cal}}{\cancel g °C}}\times\frac{4,18\;\mathrm J}{1\;\mathrm{\cancel{cal}}}\times\frac{1000\;\mathrm{\cancel g}}{1\;\mathrm{kg}}=4180\;\mathrm{\frac{J}{kg°C}}
\end{gather}
\]
A Energia Potencial é dada por
\[
\begin{gather}
\bbox[#99CCFF,10px]
{E_p=mgh} \tag{I}
\end{gather}
\]
A quantidade de calor recebida pelo corpo é dada por
\[
\begin{gather}
\bbox[#99CCFF,10px]
{Q=mc\Delta t} \tag{II}
\end{gather}
\]
A energia potencial inicial é convertida em calor no final, igualando as equações (I) e (II)
\[
\begin{gather}
E_p=Q \\[5pt]
\cancel m gh=\cancel m c\Delta t \\[5pt]
h=\frac{c \Delta t}{g}
\end{gather}
\]
substituindo os dados do problema
\[
\begin{gather}
h=\frac{4180\times 1}{9,8}
\end{gather}
\]
\[
\begin{gather}
\bbox[#FFCCCC,10px]
{h=426,5\;\mathrm m}
\end{gather}
\]
publicidade

Fisicaexe - Exercícios Resolvidos de Física de Elcio Brandani Mondadori está licenciado com uma Licença Creative Commons - Atribuição-NãoComercial-Compartilha Igual 4.0 Internacional .