Exercício Resolvido de Corrente Elétrica
publicidade
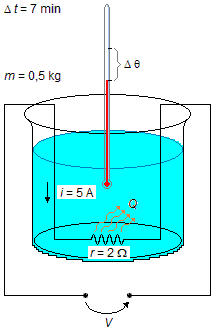
Num recipiente contendo 0,5 kg de água é colocado um resistor com 2 Ω de resistência elétrica percorrida por uma corrente elétrica de 5 A durante 7 min. Calcule a elevação de temperatura da água, supondo que não haja mudança de estado.
Dados: calor específico da água 1 cal/g°C e o equivalente mecânico do calor 1 cal = 4,2 J.
Dados do problema:
- Massa de água: m = 0,5 kg;
- Resistor: r = 2 Ω;
- Corrente elétrica: i = 5 A;
- Intervalo de tempo de aquecimento: Δt = 7 mim;
- Calor específico da água: c = 1 cal/g°C;
- Equivalente mecênico do calor: 1 cal = 4,2 J.
Quando a corrente elétrica i percorre o circuito o resistor produz um calor Q,
por Efeito Joule, que vai aquecer a água, fazendo a temperatura se elevar de um valor
Δθ (Figura 1).
Observação: Usamos o símbolo θ para a temperatura para não confundir com
t usado para o tempo.
Solução
Em primeiro lugar devemos converter o intervalo de tempo dado em minutos (min) para segundos (s) usado no Sistema Internacional (S.I.).
\[
\Delta t=7\;\cancel{\text{min}}.\frac{60\;\text{s}}{1\;\cancel{\text{min}}}=420\;\text{s}
\]
A potência dissipada no resistor é dada por
\[ \bbox[#99CCFF,10px]
{\mathscr{P}=ri^{2}}
\]
\[
\begin{gather}
\mathscr{P}=2.5^{2}\\
\mathscr{P}=2.25\\
\mathscr{P}=50\;\text{W}
\end{gather}
\]
A potência é a quantidade de energia transferida por unidade de tempo, a quantidade dissipada no
resistor será
\[ \bbox[#99CCFF,10px]
{\mathscr{P}=\frac{E}{\Delta t}}
\]
\[
\begin{gather}
E=\mathscr{P}\Delta t\\
E=50.420\\
E=21000\;\text{J}
\end{gather}
\]
Convertendo a energia dada em joules (J), usado no Sistema Internacional (S.I.), para calorias (cal)
e a massa de água dada em quilogramas (kg) para gramas (g)
\[
\begin{gather}
E=Q=21000\;\cancel{\text{J}}.\;\frac{1\;\text{cal}}{4,2\;\cancel{\text{J}}}=5000\;\text{cal}\\[10pt]
m=0,5\;\cancel{\text{kg}}.\;\frac{1000\;\text{g}}{1\;\cancel{\text{kg}}}=500\;\text{g}
\end{gather}
\]
Observação: Convertemos a energia de joules para calorias por ser uma unidade mais
conveniente de ser utilizada neste problema. Se a energia fosse deixada em joules teríamos que
converter o calor específico da água, dado em calorias por grama grau Celsius (cal/g °C), para
joules por quilograma grau Celsius (J/kg °C). Mas usualmente nos problemas o calor, que é energia
em trânsito, é dado em calorias.
O calor recebido pela água, onde não há mudança de estado, será
\[ \bbox[#99CCFF,10px]
{Q=mc\Delta \theta}
\]
a variação da temperatura da água será
\[
\begin{gather}
\Delta \theta =\frac{Q}{mc}\\
\Delta \theta=\frac{5000}{500.1}\\
\Delta \theta =\frac{5000}{500}
\end{gather}
\]
\[ \bbox[#FFCCCC,10px]
{\Delta \theta =10 °\text{C}}
\]
publicidade

Fisicaexe - Exercícios Resolvidos de Física de Elcio Brandani Mondadori está licenciado com uma Licença Creative Commons - Atribuição-NãoComercial-Compartilha Igual 4.0 Internacional .